Blog original en ingles por Denise N. Williams
Traducido por Joel Hernandez
Editado por Becky Rodriguez
¿Sabía usted que la piel es el órgano más grande del cuerpo? Cubre alrededor de 1,8 metros cuadrados1. Sirve como la capa protectora más externa del cuerpo, limitando el movimiento de moléculas dentro y fuera del cuerpo, manteniendo todos los órganos del cuerpo cerca y siendo la primera barrera defensiva contra amenazas externas. Pero su eficacia como barrera presenta algunos retos cuando queremos que los medicamentos pasen al cuerpo por medio de la piel. Algunas nuevas tecnologías están utilizando nanopartículas para ayudar a superar esos desafíos.

FIGURA 1: La piel hace un gran trabajo como una barrera entre el interior y el exterior de nuestro cuerpo (imagen de Pixabay)
La estructura de la piel es clave para su funcionamiento. Está hecha de tres capas – la epidermis, la dermis y la hipodermis – que entre otras cosas le dan a la piel cualidades duraderas y flexibles1. (Para más información sobre la composición de la piel, vea el artículo de Alicia McGeachy sobre lo que las nanopartículas de oro tienen que ver con la piel arrugada.) La figura de abajo ilustra los poros, folículos pilosos y glándulas sudoríparas en estas capas como las rutas que controlan el movimiento de moléculas dentro y fuera del cuerpo. Estas moléculas incluyen agua, sal, aceites y ahora fármacos, ya que usamos la piel para actuar como un sistema de administración de fármacos para el tratamiento de diferentes malestares1.
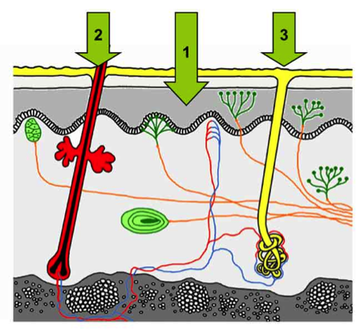
FIGURA 2: Vías de penetración del fármaco. 1) Transdermal, o por la epidermis. 2) A través de las glándulas sudoríparas. 3) Folicular, o a través de los folículos pilosos. (Imagen de Uchechi et al., 2014 1)
La aplicación directa de fármacos a la piel y su movimiento a través de la piel se denomina la administración dérmica de fármacos1-4. Los protectores solares, los ungüentos para músculos y las cremas para el acné y dermatitis son todos ejemplos de sistemas de fármacos dérmicos, aunque algunos (como ungüentos para músculos) son hechos para penetrar la piel y otros (como cremas para dermatitis) son hechos para mantenerse fuera del cuerpo1. La liberación de fármacos a través de la piel proporciona muchas ventajas sobre otras vías de suministro de fármacos tales como oral (por la boca) o inyección intravenosa (en el torrente sanguíneo). Una ventaja de la administración dérmica es que es una alternativa sin dolor a las jeringas o las píldoras difíciles de tragar. Los fármacos aplicados por vía dérmica son fáciles de auto-administrar y fáciles de eliminar si producen una reacción alérgica. A diferencia de las píldoras, los fármacos dérmicos también tienen la ventaja de que no requieren digestión en los intestinos, sino que van directamente al torrente sanguíneo después de pasar a través de la piel para que no causen reacciones intestinales negativas1.

FIGURE 3: La administración dérmica de fármacos puede ser mucho más conveniente que las píldoras o las inyecciones. (Imagen por ReqgBarc)
Aunque la administración dérmica de fármacos parece ser un método ideal para los pacientes, el diseño de fármacos que pueden ser suministrados a través de la piel es difícil. Después de todo, uno de los propósitos de la piel es impedir a las moléculas de entrar al cuerpo. Entonces, ¿cómo puede un fármaco lograr romper la barrera de la piel? Los fármacos dérmicos se mueven habitualmente entre las células de la capa epidérmica de la piel1. Para maniobrar y llegar más allá de estas células, los fármacos deben poseer ciertas características. Deben ser muy ligeros, tener ciertas propiedades de carga y ser más pequeños que unos pocos micrómetros (millonésimas de metro) para que puedan pasar entre las membranas celulares1.
Una forma en que los científicos han estado explorando la administración dérmica de fármacos es mediante el uso de nanopartículas. Como usted puede recordar, hay 1.000 nanómetros en un micrómetro, por lo que las nanopartículas definitivamente se ajustan a los requisitos de tamaño para los medicamentos dérmicos. El hecho de que sean tan pequeños generalmente se encarga de las restricciones de peso, también. Pero sólo porque una nanopartícula es lo suficientemente pequeña como para pasar por la piel, ¿significa que lo hará? ¿Cómo se aseguran los científicos que una nanopartícula quiera viajar a través de la piel? Resulta que las nanopartículas también son útiles para la administración de fármacos porque se pueden modificar para ajustarse a las características de carga necesarias.

FIGURA 4: Las nanopartículas proporcionan soluciones a algunos desafíos con el suministro dérmico de fármacos (imagen adaptada de Richard Drdul)
Una característica importante es el comportamiento anfipático. Los científicos diseñan partículas con una región polar (que atrae el agua) y una región no polar (que atrae las grasas). El comportamiento anfipático permite que las nanopartículas pasen a través de las membranas no polares de la epidermis, y luego que sean llevadas por el torrente sanguíneo polar. (Recuerde la regla química: lo similar disuelve lo similar).
Otro aspecto de la carga sobre los fármacos suministrados por las nanopartículas es la densidad de carga. La densidad de carga es la cantidad de carga eléctrica sobre la superficie de la partícula por volumen de la unidad. Si el fármaco está demasiado cargado positivamente, puede pegarse a las membranas celulares cargadas negativamente en lugar de viajar a su objetivo. Si el fármaco está demasiado cargado negativamente entonces las membranas celulares repelen el fármaco y eso también puede prevenir la entrega. Así que la densidad de la carga tiene que ser precisa para que el fármaco pase entre las células.
Dos factores más en el diseño de nanopartículas que son importantes para el suministro de fármacos son el potencial zeta y la hidrofobicidad. El potencial zeta tiene que ver con el potencial eléctrico entre las moléculas, e influye en si las partículas permanecen estables o agregadas en grupos inútiles o incluso dolorosos. La hidrofobicidad es la medida de cuánto “disgusto” una partícula tiene por el agua. Un fármaco muy hidrófoba no se disolverá en el agua, lo cual significa que no será capaz de viajar a través del torrente sanguíneo, que se compone principalmente de agua. Para evitar que el fármaco forme hinchazónes dolorosos dentro del cuerpo y para ayudarlo a viajar a través del cuerpo a su objetivo deseado, el fármaco de las nanopartículas necesita ser hidrófilo (aficionado al agua).
Hay una variedad de sistemas de fármacos dérmicos actualmente en desarrollo utilizando nanopartículas. Un tipo de nanopartícula que está siendo investigado como un sistema de transporte de fármacos para el suministro dérmico son las nanopartículas de lípidos sólidos (“SLN” por sus siglas en inglés) (véase más adelante). Las SLN son estructuras con moléculas lipídicas (grasas) en el exterior y un área interior para transportar fármacos1-3. Estas partículas pueden consistir de lípidos fisiológicos y biodegradables que viajan pasivamente entre las células por ser hidrofóbicas en el exterior, así como las membranas de células que están rebasando2,3. Se puede pensar en las SLN como camiones camuflados: Los asientos del camión están llenos de moléculas de fármacos y su camuflaje de superficie lipídica les ayuda a pasar por los lípidos alrededor de las células de la capa externa de la piel. Actualmente, las SLN están siendo implementados como sistemas de administración de fármacos para algunos tipos de protección solar, condiciones de dermatitis, hiperpigmentación, artritis y legiones cutáneas2,5.
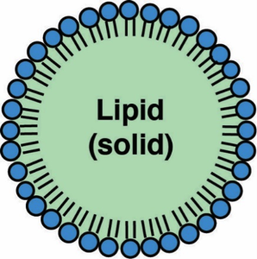
FIGURA 5: Diagrama de una nanopartícula de lípidos sólida (SLN) (imagen de Pratibha et al., 20142) (lípidos – lipid, sólido – solid)
Debido a que contienen el fármaco completamente dentro de su caparazón de lípidos, las SLN ofrecen una solución para el problema de los fármacos hidrofóbicos que ordinariamente no sería capaces de moverse a través del torrente sanguíneo. Además de transportar los fármacos, las SLN protegen a los fármacos de la degradación hasta alcanzar su objetivo1-3. Pueden penetrar más profundamente en los folículos capilares que otros fármacos dérmicos debido a su tamaño nano1. Pueden incluso ser liofilizados y almacenados para uso futuro, permitiendo una vida útil más larga y un transporte más fácil del fármaco desde el distribuidor al paciente2.
Estas SLN suenan increíbles, pero hay algunos inconvenientes. Los lípidos que rodean a la partícula pueden crecer con el tiempo, transformándose en una rejilla de cristal y un gel que podría prevenir la liberación del fármaco o incluso ser tóxico1-3. También hay un límite de capacidad de carga del fármaco dependiendo de la relación de tamaño entre la SLN y el fármaco2,3. (Volviendo a nuestro camión camuflado: sólo se puede poner tanta gente en el camión como hay asientos y tal vez espacio en el piso, ¿verdad? Lo mismo con estas SLN. Tienen un área interior limitada para el transporte de moléculas de fármacos, así que usted debe tener un medicamento tan fuerte como sea posible para que la cantidad que se ajusta en la SLN sea suficiente para hacer el trabajo).
Los parches de grafeno son otro sistema de transporte de fármacos bajo investigación científica para su uso en la administración dérmica de fármacos. En junio de 2016, Hyunjae Lee y sus colaboradores publicaron un documento exponiendo la preparación de un parche de grafeno que se utilizará para el suministro de fármacos para la diabetes (que se muestra a continuación)4. El parche tiene capacidades tanto de sensor como de suministro de fármacos, lo cual significa que sólo se necesita de un dispositivo para diagnosticar como para tratar al paciente. Los sensores miden la temperatura, la acidez, la humedad y la concentración de glucosa, que a su vez envían una respuesta eléctrica a la tecnología de suministro de fármacos en el parche. El componente de administración de fármacos utiliza la respuesta eléctrica como un calentador para fundir microagujas poliméricas cargadas con el fármaco de diabetes para su administración a la piel del paciente4,6. En esencia, cuando la concentración de glucosa de un paciente cambia, el fármaco se administra como corresponde.

FIGURA 6: La ilustración de un parche de grafeno propuesto para administrar medicamentos para diabetes (Imagen de Torrice, 20166) ( detección de glucosa – glucose detection, administración fármaco – drug delivery)
La ventaja de este sistema de administración de fármacos para la diabetes es que es más compatible con el paciente que las tecnologías actuales porque el paciente ya no tendrá que picar el dedo para una lectura de glucosa. El parche puede detectar la cantidad de fármaco que el paciente necesita por medir los niveles de glucosa, y puede permanecer encendido para la detección y suministro del fármaco automático, inmediato, y de largo plazo. Sin embargo, al igual que la capacidad limitada de las SLN para transportar gran cantidad de fármacos a los objetivos previstos, estas microagujas sólo pueden transportar pequeñas cantidades de moléculas de fármacos, requiriendo de un fármaco de alta potencia para que sea realmente útil4.
El uso propuesto y real de las nanopartículas como vehículos de suministro de fármacos se está volviendo cada vez más popular. Están siendo investigadas para tratar una gama de trastornos incluyendo la diabetes, el acné, el eczema y el artritis1. Varios sistemas diferentes de nanopartículas son prometedores para estas aplicaciones, incluyendo (pero no limitadas a) las nanopartículas de lípidos sólidas y los parches de grafeno mencionados arriba, pero también los liposomas, el sílice, los polímeros y los dendrímeros1,2. Más investigación sobre estas nanopartículas de liberación de fármacos con un enfoque en la afinidad y eficacia del fármaco pronto traerá más de estas tecnologías compatibles con los pacientes al mercado.
RECURSOS EDUCATIVOS
- NISEnet: Medicina-nano en Foro de Salud – en inglés.
- National Nanotechnology Infrastructure Network: Monitoreando Glucosa en la Sangre actividad en inglés.
REFERENCIAS
- Uchechi, O., Ogbonna, J. & Attama, A. “Application of Nanotechnology in Drug Delivery,” in Nanotechnology and Nanomaterials edited by Ali Demir Sezer. 2014. DOI: 5772/58672
- Kakadia, P. & Conway, B. Solid Lipid Nanoparticles: A Potential Approach for Dermal Drug Delivery. American Journal of Pharmacological Sciences, 2014, 2(5A), 1-7. doi: 12691/ajps-2-5A-1
- Wilczewska, A. et al. Nanoparticles as Drug Delivery Systems. Pharmacological Reports, 2012, 64, 1020-1037. doi: 1016/S1734-1140(12)70901-5
- Lee, H. A graphene-based electrochemical device with thermoresponsive microneedles for diabetes monitoring and therapy. Nature Nanotechnology, 2016, 11, 566- 574. doi: 10.1038/nnano.2016.38
- Yeh, M. et al. Dermal delivery by niosomes of black tea extract as a sunscreen agent. International Journal of Dermatology. 2013, 52(2), 239-45. doi: 1111/j.1365-4632.2012.05587.x
- Torrice, M. Graphene patch could help patients manage diabetes. Chemical &Engineering News, 2016, 94(13), 5. http://cen.acs.org/articles/94/i13/Graphene-patch-help-patients-manage.html