Originalmente publicadoen inglés
Publicado el 11 de junio del 2018
Traducido por Regina González Lona,
Editado por Wilanyi R. Alvarez Reyes y Lissett G. Diaz
La mayoría de nosotros estamos familiarizados con el concepto de “efectos secundarios”. Aquí es cuando algo que está diseñado para ser útil termina teniendo algún daño que lo acompaña. Para los pacientes con cáncer, los medicamentos contra el cáncer pueden salvarles la vida, literalmente. Los beneficios de usar estos medicamentos son evidentes para cualquier persona cuyo cáncer haya entrado en remisión gracias a su uso. Es bien sabido que estos medicamentos también pueden tener algunos efectos secundarios desagradables, sin embargo, las personas aún eligen usarlos porque los beneficios de curarse superan los problemas (y, por supuesto, los investigadores continúan buscando formas de reducir esos efectos negativos). La medicina no es la única área donde esto sucede: hay muchas tecnologías que tienen muchos beneficios para su uso, pero pueden tener algunos efectos secundarios potencialmente malos. Las nanopartículas son un ejemplo; tienen muchos usos asombrosos para los productos de consumo, pero a veces pueden tener impactos dañinos en los organismos ambientales. Uno de los objetivos del Centro de Nanotecnología Sostenible (CSN por sus siglas en inglés) es tratar de encontrar opciones para diseñar nanopartículas de modo que se puedan reducir esos impactos nocivos.

Un paso importante hacia el objetivo de diseñar nanopartículas más ecoamigables es averiguar cómo interactúan las diferentes nanopartículas con los diferentes organismos del medio ambiente. Para hacer esto, investigamos las interacciones a nivel molecular. El objetivo es poder predecir las interacciones y cualquier toxicidad potencial de las nanopartículas con los organismos, y luego usar ese conocimiento para diseñar nanopartículas de una manera que mitigue el riesgo ambiental.
Como puede imaginar, este es un gran objetivo, ¡con mucha investigación para realizar un seguimiento! Un grupo de investigadores del CSN publicó recientemente un artículo cuyo objetivo era resumir lo que se sabe sobre el funcionamiento de la toxicidad de las nanopartículas y describir las formas en que las nanopartículas podrían rediseñarse para reducir los efectos secundarios ambientales.1 Los tres principales mecanismos de toxicidad de las nanopartículas son:
- nanopartículas que se unen al exterior de una célula
- nanopartículas que se disuelven para liberar iones tóxicos
- nanopartículas que generan especies reactivas de oxígeno (ROS por sus siglas en inglés) dañinas
Dado que la toxicidad potencial de una nanopartícula depende tanto del tipo de nanopartícula como del organismo con el que interactúa, cada uno de estos tres tipos de toxicidad puede ser importante en diferentes situaciones. Al rediseñar una nanopartícula, los científicos primero tienen que identificar el principal mecanismo de toxicidad, porque las estrategias para reducir la toxicidad, por supuesto, dependerán de la fuente de toxicidad. Se han realizado algunas investigaciones sobre el rediseño de nanopartículas, pero esperamos que nuestro artículo inspire a más científicos a evaluar algunas de las estrategias de rediseño con diferentes modelos de nanopartículas para poder hacer mejores predicciones sobre lo que funcionará. La figura 2 ofrece una descripción general rápida de la multitud de estrategias de rediseño de las que hablamos en el documento.
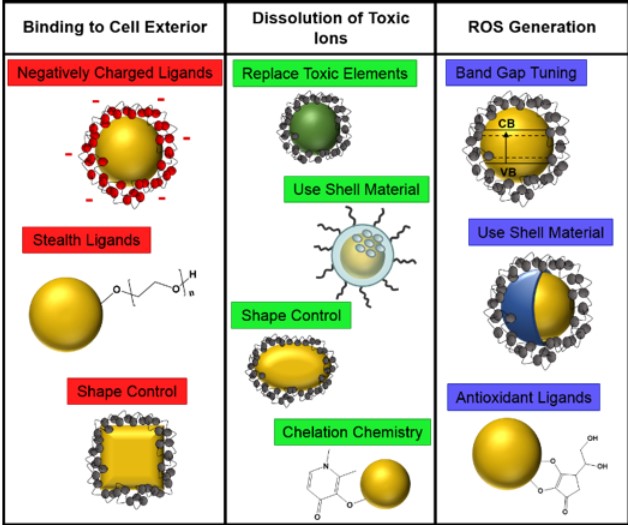
Unión al exterior de la célula
Las nanopartículas que se adhieren a la superficie de una célula pueden romper la membrana de la célula, lo que puede matarla. Dependiendo del tipo de célula, las nanopartículas también pueden ingresar a la célula después de unirse y potencialmente causar daño de esa manera. Hay varias opciones para rediseñar una nanopartícula para reducir su capacidad de unión. Uno implica cambiar la carga superficial de la nanopartícula. Sabemos que la mayoría de las células tienen una carga negativa en su superficie celular, y sabemos que lo similar repele lo similar (al igual que con los imanes). Por lo tanto, si las nanopartículas están diseñadas para tener cargas superficiales negativas, serán menos capaces de unirse a la superficie celular y, por lo tanto, no pueden dañar las células debido a la unión.
En otro trabajo del CSN (descrito en esta publicación de blog), demostramos que el uso de nanopartículas de oro con una carga superficial positiva generaba mucha unión con la superficie bacteriana y, en consecuencia, mucha toxicidad.2 Con nanopartículas de oro que se hicieron con una carga superficial negativa, apenas se observó unión y las nanopartículas no mostraron toxicidad para las bacterias. Esto demuestra que ser capaz de rediseñar una nanopartícula para que tenga una carga negativa puede reducir su impacto en las células bacterianas.

Disolución
Otra forma en que las nanopartículas pueden ser tóxicas para los organismos ocurre cuando se disuelven en líquido, lo que libera iones (moléculas cargadas) en el medio ambiente. Estos iones pueden interactuar con las células y ser absorbidos por ellas, a veces con efectos nocivos. Una forma de rediseñar las nanopartículas para reducir la liberación de iones tóxicos es reemplazar los elementos que son tóxicos en su forma iónica con algo menos tóxico. Este enfoque se ha investigado con una nanopartícula modelo que se utiliza a menudo en el CSN: el óxido de litio, níquel, manganeso y cobalto (NMC). Como discutimos en esta publicación de blog y en este episodio de podcast, sabemos que el NMC es tóxico para la bacteria Shewanella oneidensis porque libera iones de níquel y cobalto en la solución3. contenido de níquel y cobalto) para ver si sería menos tóxico.4 Para medir la toxicidad, utilizamos una técnica llamada espirometría, que analiza la cantidad de oxígeno que utilizan las bacterias. Como se muestra en el gráfico a continuación, resultó que después de la exposición a los materiales NMC enriquecidos con manganeso (línea verde), S. oneidensis volvió a usar la misma cantidad de oxígeno que las bacterias que no estuvieron expuestas a nanopartículas (línea negra). ) más rápidamente que los expuestos a NMC con más níquel y cobalto (líneas azul y roja).

Especies reactivas de oxígeno
Otra forma en que las nanopartículas pueden ser tóxicas es en su capacidad para producir especies reactivas de oxígeno (ROS). Como su nombre lo indica, las ROS son formas de oxígeno altamente reactivas (descritas brevemente aquí), lo que significa que interactúan con otros materiales muy fácilmente. Son tan reactivos que pueden reaccionar con muchos componentes celulares importantes diferentes, como los lípidos en la membrana celular, varias proteínas y el ADN. Para reducir la cantidad de ROS que generan, las nanopartículas se pueden recubrir con una cubierta hecha de un material menos propenso a la producción de ROS. Por ejemplo, en un estudio, los científicos demostraron que agregar una capa de sulfuro de zinc a los puntos cuánticos de seleniuro de cadmio redujo su producción de ROS sin cambiar la funcionalidad de los puntos cuánticos.5 Esto demuestra que el recubrimiento puede ser un método efectivo para reducir los impactos en los organismos debido a generación de ROS.

Estos son solo algunos ejemplos de las muchas formas en que se pueden rediseñar las nanopartículas para reducir sus interacciones con (y su potencial toxicidad) con los organismos del medio ambiente. Todavía queda mucho trabajo por hacer para comprender las diferentes formas en que las nanopartículas pueden ser potencialmente tóxicas para los organismos, y hay estudios en curso en el CSN para comprender mejor estos mecanismos. Sin embargo, también tenemos suficiente conocimiento que ahora se puede aplicar para investigar los diversos métodos mediante los cuales se pueden mitigar estos efectos secundarios, que es un área más nueva por explorar en el campo de las nanopartículas. Es importante recordar que las nanopartículas tienen grandes beneficios para diferentes productos de consumo y tecnologías médicas, pero al rediseñarse para mejorar su impacto ambiental, podemos trabajar para que el uso de nanopartículas sea más sostenible a largo plazo.
Referencias
- Buchman, J. T.; Hudson-Smith, N. V; Landy, K. M.; Haynes, C. L. Understanding Nanoparticle Toxicity Mechanisms To Inform Redesign Strategies To Reduce Environmental Impact. Accounts of Chemical Research, 2019, 52, 1632–1642. doi: doi.org/10.1021/acs.accounts.9b00053
- Feng, Z. V.; Gunsolus, I. L.; Qiu, T. A.; Hurley, K. R.; Nyberg, L. H.; Frew, H.; Johnson, K. P.; Vartanian, A. M.; Jacob, L. M.; Lohse, S. E.; Torelli, M. D.; Hamers, R. J.; Murphy, C. J.; Haynes, C. L. Impacts of Gold Nanoparticle Charge and Ligand Type on Surface Binding and Toxicity to Gram-Negative and Gram-Positive Bacteria. Chemical Science, 2015, 6, 5186–5196. doi: 10.1039/C5SC00792E
- Hang, M. N.; Gunsolus, I. L.; Wayland, H.; Melby, E. S.; Mensch, A. C.; Hurley, K. R.; Pedersen, J. A.; Haynes, C. L.; Hamers, R. J. Impact of Nanoscale Lithium Nickel Manganese Cobalt Oxide (NMC) on the Bacterium Shewanella Oneidensis MR-1. Chemistry of Materials, 2016,28, 1092–1100. doi: https://doi.org/10.1021/acs.chemmater.5b04505
- Gunsolus, I. L.; Hang, M. N.; Hudson-Smith, N. V; Buchman, J. T.; Bennett, J. W.; Conroy, D.; Mason, S. E.; Hamers, R. J.; Haynes, C. L. Influence of Nickel Manganese Cobalt Oxide Nanoparticle Composition on Toxicity toward Shewanella Oneidensis MR-1: Redesigning for Reduced Biological Impact. Environmental Sciece: Nano, 2017, 4, 636–646. doi: 10.1039/C6EN00453A
- Ipe, B. I.; Lehnig, M.; Niemeyer, C. M. On the Generation of Free Radical Species from Quantum Dots. Small, 2005, 1, 706–709. doi: 10.1002/smll.200500105